Silikon-Implantate werden im Organismus chemisch aktiv
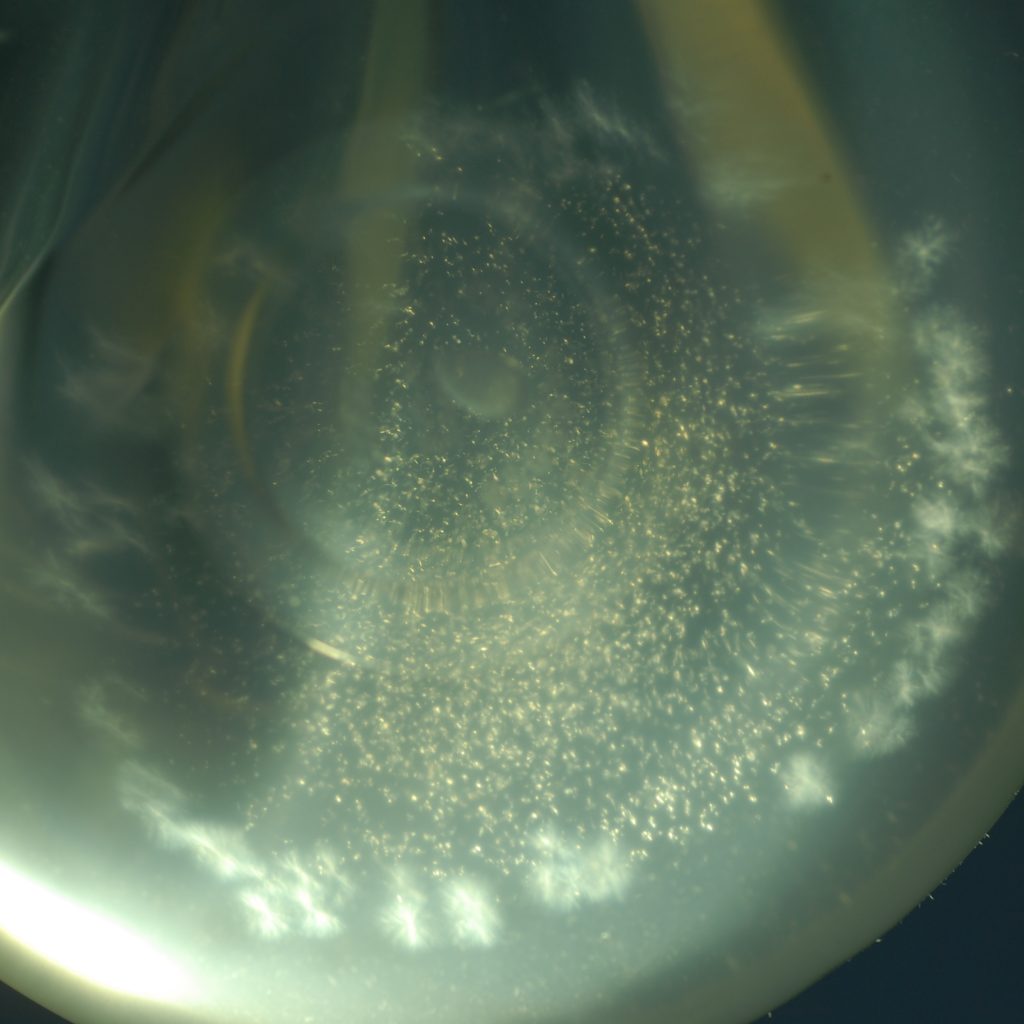
„Präzipitate im Silikongel“ makroskopisch
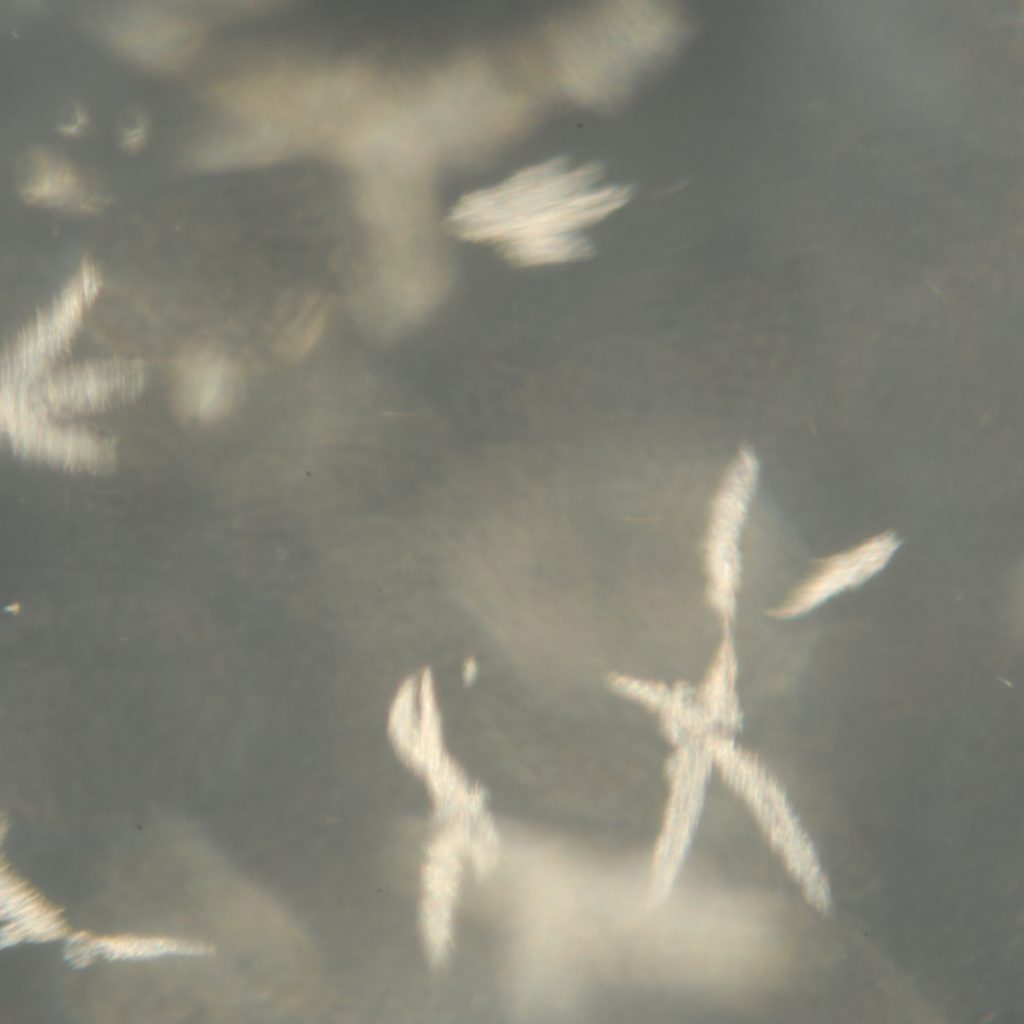
„Präzipitate im Silikongel“ mikroskopisch
Silikon-Implantate besitzen generell eine äußere Hülle aus Silikon-Gummi (Silikon-Elastomer). Diese ist durchlässig für organische Chemikalien incl. Biomoleküle und Umweltgifte (z.B. polychlorierte Benzole: PCBs). Diese reichern sich durch Diffusion im Innern der Implantate während des Aufenthaltes im Bioorganismus an – analog zum Fettgewebe (siehe auch „silicone wristbands“). Dies kann bewiesen werden durch optischen Nachweis von Kristallbildung innerhalb von 24 Std. in den Silikongelen der Implantate nach Entfernung.
Durch analytische Verfahren wurden bereits einzelne Chemikalien identifiziert, z.B. Phospholipide, Steroide, PCBs, Propofol. Die Frage ist, wie werden diese Chemikalien im Innern der Gele verändert, z.B. durch Sauerstoff (siehe Sojaöl-Implantate) und durch Katalyse infolge von verbliebenem Platin, und ab welchem Zeitpunkt gelangen die Chemikalien zurück in den Organismus des „Wirtes“? (Bestimmte PCBs stehen im Zusammenhang mit der Entwicklung von Non-Hodgkin-Lymphomen.) In Bezug auf ALCL können diese Beobachtungen und die daraus resultierenden Fragen nicht ignoriert werden.
Davon zunächst unabhängig ist in ca. 10% der entfernten Implantate mit intakter äußerer Hülle „Wachstum“ zu beobachten, d.h. zum Zeitpunkt der Implantat-Entfernung sind die Gele optisch durchsichtig. Nach Aufbewahrung im Trockenen bei Raumtemperatur entwickeln sich während einer Zeitspanne von 6 -8 Wochen im Innern die im Poster (VAAM 2016/Jena) gezeigten, mit freiem Auge erkennbaren optischen Einschlüsse. Sie wachsen so zu sagen heran! Der Zeitbedarf ist deutlich zu unterscheiden von der vorgenannten Kristallbildung (24 Std. nach Explantation). Es ist ein anderes Phänomen. Wir vermuten biologisches Wachstum im Innern der Implantate.
Die Voraussetzungen für biologisches Wachstum im Innern der entfernten Implantate mit intakter Silikon-Hülle sind:
- Kontamination der Silikon-Komponenten mit Sporen (Pilze, Bakterien) bei der Herstellung, bestätigt durch Konidien-Nachweis (Institut Fresenius, Tab.1 im Poster),
- unzureichende Sterilisation des Endproduktes (trockene Hitze 100°C statt Autoklavierung mit Dampf 121°C bei 2 atm ),
- Nährstoffangebot (siehe oben organische Chemikalien),
- geeignete Wachstumsbedingungen, z.B. 36°C, gesättigte Wasserdampf- bzw.- Sauerstoff-Atmosphäre im Innern des Körpers, bei Implantat-Entfernung Änderung der Wachstumsbedingung und Bildung von sichtbaren Sporenträgern.
Versuche eines DNA-Nachweises in den Einschlüssen per PCR blieben mit der Ausnahme der Untersuchung des Holz-Institutes Dresden (siehe Poster VAAM 2016/Jena Tab.1) erfolglos. Hierfür kann die Interaktion der Polydimethylsilikon-Moleküle (PDMS) mit der DNA bemüht werden. Prof. Storsberg vom Fraunhofer-Institut Potsdam hat aus entsprechenden Untersuchungen eine ungewöhnliche thermische Stabilität der DNA im Silikon bei 160°C festgestellt. Es wäre Aufgabe des BfArM und der zuständigen Benannten Stellen gewesen, nach Hinweis auf das vermutete biologische Wachstum die Sterilisationsbedingungen für Silikon-Implantate zu überprüfen. Der Hinweis eines Herstellers auf Kontrolle des Sterilisationsverfahrens mit Sporen von B. stearothermophilus greift zu kurz, da der Keim am Ende des Herstellungsverfahrens eingesetzt wird. Es handelt sich um ein Surrogat. Das Überleben anderer extremophiler Sporen von Pilzen und Bakterien, eingebettet in die PDMS-Matrix beim Herstellungsverfahren, ist damit nicht mit der notwendigen Sicherheit ausgeschlossen.
Biologisches Wachstum im Innern der Implantate, d.h. die Bildung eines primär optisch nicht sichtbaren Mycels, bedeutet: Stoffwechsel durch Verwertung der Nährstoffe und Bildung von Abbau-Produkten. Erfahrungsgemäß und aufgrund der Lehren der Mikrobiologie können Letztere im menschlichen Organismus toxisch wirken. Sie sind damit pathogen.
Toxin-Entstehung – auf welchem Wege auch immer – im Innern von Silikon-Implantaten kann auch das bevorzugte Auftreten des ALCL bei texturierten Implantaten erklären:
Das in die „wells“ (Brunnen) eingewachsene und somit fixierte Kapselgewebe ist von 5 Seitenwänden des chemisch „leitfähigen“ Silikon-Elastomers umgeben, wie der Finger in der Sahne. Damit können die aus den Wänden austretenden Toxine in den Lumina der Textur höhere Konzentrationen erreichen. Gleichzeitig ist damit erklärt, warum ALCL auf der Implantat-Seite der Gewebskapsel entsteht. Die Situation des Kapselgewebes bei glatten Silikon-Oberflächen ist grundsätzlich günstiger in Bezug auf Toxin-Anreicherung an der Implantat-Oberfläche.
Toxin-Bildung im Innern von Silikon-Implantaten muss auch in Bezug auf alle bisher nicht abschließend geklärten unerwünschten Wirkungen dieser Medizin-Produkte als ursächlich in Betracht gezogen werden, insbesondere bei systemischen Erkrankungen die unter dem Begriff Silikon-Krankheit zusammengefasst werden können.
